TRIM67基因缺失可以减缓肥胖诱导的非酒精性脂肪肝的进展
2022年7月,本实验室毕业研究生魏小丽为共同第一作者在国际学术期刊《International Journal of Molecular Sciences》在线发表我校动物医学院实验动物疾病模型研究室题为“Loss of TRIM67 Attenuates the Progress of Obesity-Induced Non-Alcoholic Fatty Liver Disease”的研究论文。 该期刊最新影响因子为IF=6.208。
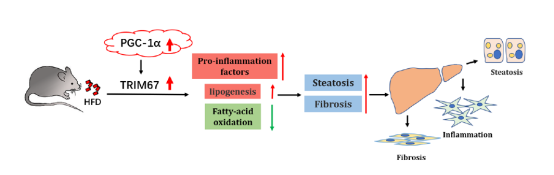
该研究利用基因敲除的手段,基于TRIM蛋白家族成员TRIM67,建立了高脂饮食诱导的用于非酒精性脂肪肝研究的实验动物模型,并首次揭示了TRIM67蛋白在非酒精脂肪肝发展过程中响应并调控肝细胞脂肪积累、炎症反应及纤维化形成的作用机制。
目前,肥胖症发病率以前所未有的速度增长,正在席卷全球。肥胖与非酒精性脂肪性肝病(NAFLD)的发生和进展密切相关。NAFLD被认为是慢性肝病的最常见原因,影响全球约25%的普通人群。NAFLD作为一种临床综合征,是一系列肝脏疾病的综合表现,包括从单纯的肝脏脂肪变性即单纯性非酒精性脂肪肝(Nonalcoholic fatty liver, NAFL)到非酒精性脂肪性肝炎(NASH)及肝硬化乃至肝癌的一系列病变。因此,深入研究NAFLD疾病发生发展中的调控机制,并基于此建立合适的动物疾病模型具有良好的理论基础和诱人的前瞻性。
TRIM67是三结构域(Tripartite Motif, TRIM)蛋白家族的成员之一,TRIM家族是RING结构域E3泛素连接酶的一个亚类,大多数蛋白成员都具有E3泛素连接酶活性,在具有多种生物学功能。在这项研究中,我们发现TRIM67在肥胖诱导的NAFLD的发展和进展中发挥了新的作用。高脂饮食/肥胖可促进TRIM67的表达并激活肝脏炎症,积累肝脂和NAFLD的进展,而缺乏TRIM67可防止这些过程。此外,我们的研究结果进一步表明PGC-1a在调节TRIM67对肥胖的反应中发挥了作用。除了在大脑中,TRIM67在其他一些器官中表达,我们的数据让我们离了解TRIM67的生物学功能更近了一步,并提供了新的方面。
文章链接:https://www.mdpi.com/1422-0067/23/13/7475